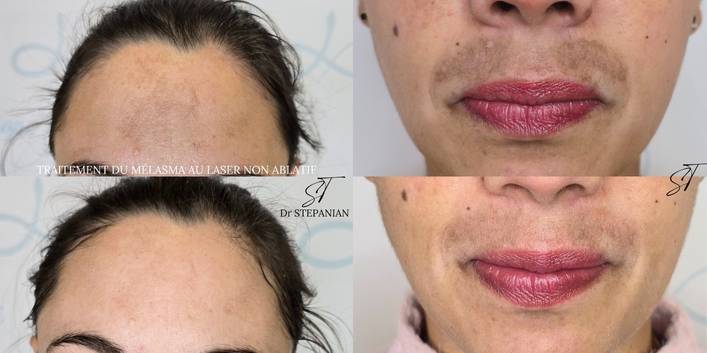
Le mélasma est une hyperpigmentation acquise du visage, multifactorielle et souvent résistante aux traitements classiques. Le laser fractionné Erbium:Glass (Er:Glass) a émergé comme une alternative efficace grâce à sa capacité à induire un remodelage dermique sans destruction extensive de l’épiderme. Nous rapportons ici deux cas de mélasma dermique et mixte traités par laser Er:Glass 1550 nm fractionné, en association avec des soins topiques spécifiques et une photoprotection stricte.
Introduction
Le mélasma est une dyschromie chronique, caractérisée par des plaques hyperpigmentées symétriques, principalement sur les zones exposées au soleil. Son étiopathogénie implique une interaction complexe entre facteurs hormonaux, exposition solaire, inflammation cutanée et susceptibilité génétique (1). Le traitement du mélasma reste difficile, avec un risque élevé de récidive. Les lasers fractionnés non ablatifs, comme l’Erbium:Glass à 1550 nm, ciblent principalement le derme moyen et profond, stimulant la néocollagénèse et modulant la production de mélanine (2,3).
Physiopathologie
Le mélasma est une hypermélanose acquise chronique, caractérisée par une pigmentation brunâtre symétrique du visage. A l’échelle cellulaire et moléculaire, il résulte d’une dérégulation de la mélanogenèse, processus par lequel les mélanocytes produisent de la mélanine à partir de la L-tyrosine, sous l’action de l’enzyme tyrosinase et de ses cofacteurs (TYRP1, TYRP2).
Biologie cellulaire de la mélanogenèse perturbée
Dans le mélasma, on observe une stimulation aberrante des mélanocytes épidermiques et dermiques, souvent associée à une hyperactivité des mélanosomes, organites spécialisés dans la synthèse, le stockage et le transfert de mélanine. Le transfert mélanocytaire aux kératinocytes est également augmenté, expliquant la surcharge pigmentaire épidermique.
Des études en microscopie électronique ont montré une densité accrue de mélanosomes, souvent de type IV (grands et fortement pigmentés), dans les kératinocytes basaux des zones atteintes.
Facteurs hormonaux et régulation transcriptionnelle
Les hormones stéroïdiennes, notamment les œstrogènes et la progestérone, moduleraient l’expression de gènes clés impliqués dans la pigmentation. L’activation du récepteur des œstrogènes (ER-α) dans les mélanocytes entraîne l’induction de MITF (Microphthalmia-Associated Transcription Factor), facteur de transcription central de la mélanogenèse, régulant l’expression de la tyrosinase, TYRP1 et TYRP2.
Cette voie renforcée par les fluctuations hormonales (grossesse, contraceptifs oraux), qui activent des éléments cis-régulateurs dans les promoteurs des gènes pigmentaires.
Biochimie des voies inflammatoires et oxydatives
L’implication de l’inflammation chronique dans le mélasma est illustrée par l’activation persistante de voies comme NF-kB (Nuclear Factor kappa-light-chain-enhancer of activated B cells). Ce facteur de transcription pro-inflammatoire favorise la production de cytokines (IL-1, TNF-α), qui stimulent indirectement les mélanocytes via la cascade des MAP kinases et augmentent l’expression de la tyrosinase.
La stimulation chronique de PKC-β (protéine kinase C bêta), isoforme fortement exprimée dans le mélasma, agit en amont pour phosphoryler des protéines de signalisation comme ERK et CREB, ce qui accentue encore l’activité mélanocytaire.
De plus, un stress oxydatif accru a été observé dans les tissus affectés, avec accumulation de radicaux libres (ROS), qui activent les voies de signalisation pigmentaires et perturbent les mécanismes antioxydants endogènes (glutathion peroxydase, catalase, superoxyde dismutase…).
Vascularisation et microenvironnement dermique
L’hypervascularisation dermique, démontrée par une densité accrue de capillaires CD31+, est une caractéristique du mélasma. Les cellules endothéliales libèrent du VEGF (vascular endothelial growth factor) mais aussi de l’endothéline-1 (ET-1), un puissant agoniste des récepteurs ETA sur les mélanocytes, stimulant leur prolifération et leur activité tyrosinase-dépendante.
Le cross-talk cellulaire entre kératinocytes, fibroblastes, cellules endothéliales et mélanocytes joue un rôle central dans l’entretien du processus pigmentaire.
Perspectives génétiques et épigénétiques
Bien que le mélasma ne suive pas une hérédité mendélienne stricte, des prédispositions génétiques ont été identifiées : polymorphismes dans les gènes du récepteur de la mélanocortine (MC1R), de la tyrosinase ou encore dans ceux régulant la réponse aux UV (comme POMC; précurseur de l’α-MSH).
Des modifications épigénétiques, telles que l’hypométhylation des promoteurs de gènes pigmentaires ou l’altération de l’expression de microARNs (comme miR-434-5p, impliqué dans la régulation négative de la tyrosinase), pourraient expliquer la chronicité et la récidive du mélasma malgré les traitements.
Histologie
Histologiquement, le mélasma montre :
- Une hyperpigmentation basale épidermique
- Une présence accrue de mélanophages dermiques
- Un amincissement de la membrane basale
- Une élévation de l’activité des fibroblastes et une augmentation de collagène IV autour des capillaires dermiques (7)
La présence de mélanophages justifie une approche ciblant le derme, comme le traitement par laser non ablatif Er:Glass.
Mécanismes d’action du laser Erbium:Glass dans le traitement du mélasma
Le laser Erbium:Glass (longueur d’onde 1540-1550 nm) agit par photothermolyse fractionnée non ablative, ciblant principalement l’eau intracellulaire. Il induit des microzones de coagulation thermique dans le derme moyen à profond (jusqu’à 1000 µm), sans destruction de l’épiderme.




4 commentaires
Apres 25 ans de pratique, j’ai des bons resultats sur le Melasma avec peeling TCA, Photoled, et aussi avec mon Laser Icon 1540 . Les cremes et la photoprotections sont tjrs necessaires, le grand probleme etant la recidive quand l’été reviens…
Merci beaucoup pour votre retour et pour ces questions très pertinentes.
Je préciserai prochainement ces résultats en partageant les photographies avant/après à 1 an, chez les mêmes patientes, toujours après une séance unique, ce qui permettra d’apprécier non seulement l’efficacité initiale mais surtout la stabilité du résultat dans le temps, élément fondamental dans la prise en charge du mélasma.
De manière plus générale, dans notre expérience, il est raisonnable d’annoncer aux patients un protocole moyen de 2 à 5 séances, espacées de 6 à 8 semaines, pour espérer s’approcher d’une amélioration de l’ordre de −60 à −70 % du score MASI, ce qui constitue déjà un endpoint clinique pertinent dans cette pathologie chronique. Une séance unique peut parfois donner des résultats surprenants, mais elle ne doit pas être présentée comme la règle.
Concernant les paramètres énergétiques, il est important de souligner qu’il reste aujourd’hui complexe d’établir une équivalence stricte des réglages (fluence, durée d’impulsion, densité) entre les différentes plateformes de laser Erbium:Glass fractionné. L’expérience clinique, ainsi que les échanges avec d’autres confrères, montrent clairement que des fluences identiques exprimées en J/cm² ne produisent pas nécessairement le même effet biologique selon les marques, en raison de différences technologiques majeures : profil et homogénéité du faisceau, diamètre réel du spot, mode de fractionnement, empilement des microfaisceaux, ou encore systèmes de délivrance de l’énergie.
Cela souligne un enjeu majeur pour notre discipline : nous, praticiens en médecine esthétique, devons aller vers une meilleure harmonisation et une recherche d’équivalences inter-machines, afin de pouvoir proposer à terme des protocoles thérapeutiques plus universels, génériques et reproductibles, indépendamment des plateformes utilisées. Cette standardisation est essentielle, tant pour la comparaison des résultats entre équipes que pour la construction de recommandations scientifiques solides.
Dans l’attente de cette harmonisation, notre approche reste volontairement pragmatique et clinique, fondée sur la réponse tissulaire observée, la tolérance cutanée et la prévention du rebond pigmentaire, plutôt que sur des valeurs chiffrées transposables de manière absolue. Les paramètres sont donc ajustés de façon progressive, avec une inflammation contrôlée et mesurée, condition indispensable à la sécurité et à l’efficacité dans cette indication à haut risque pigmentaire.
Cette variabilité inter-machines explique également notre choix de ne pas figer un « protocole chiffré universel », mais plutôt de proposer une philosophie thérapeutique structurée.
Je vous remercie encore pour cet échange scientifique particulièrement constructif.
Bonjour
J’ai eu une amélioration signicative sur deux patientes dqns cette indication dès la première scéance
phototype 3 W 11j/cm2 Dp : 3 ms impulsion 1 MODE / CONTINUE énergie cumulée 170 J
j ai fait deux séances à un mois.
Merci pour ce bel article complet et résultats encourageants qui remet le laser en perspective dans cette indication difficile! Pourriez vous m’être plus indicatif sur le traitement appliqué concernant le « dosage » de l’énergie délivrée sur la zone (qui dépend je sais du stade et degré lésion et phototype), et selon votre expérience concernant le nombre de séances moyen pour arriver à un résultat satisfaisant? En général, ou sur ces 2 cas présentés.
Si je lis bien votre article vous présentez de très bons résultats de diminutions score MASI avec 1 seule séance de -70% cas 1 et -40% cas 2 et recul à 6 mois.
Serait il possible de savoir dans ces 2 cas précis 1 et 2 les paramètres énergétiques utilisés (Fluence en Joules, durée de tir en ms, mode continu ou point par point, fluence totale délivrée sur la zone traitée,etc…) et par exemple si vous avez plus de recul sur ces 2 cas, avez vous fait des séances supplémentaires et combien et à quel intervalle, sur cas 1 éventuellement? mais surtout cas 2 qui n’était qu’à 40% ? Et en général combien de séances en moyenne faut il annoncer au patient pour en moyenne s’approcher des -70% qui est un bon début d’ endpoint à atteindre dans cette pathologie difficile.
Merci pour votre retour