Technique alternative à la chirurgie classique pour corriger les effets du vieillissement, basée sur la diffusion d’ultrasons de haute intensité au sein des tissus cutanés profonds et le SMAS, la technique HIFU se présente comme une excellente technique anti-relâchement, sans grande gêne, capable d’induire une néocollagénèse et élastogénèse rapide, permettant un effet liftant durable et ce, dès l’âge moyen de 30 ans. La compréhension des principes physiques sous-jacents permet d’appréhender le fonctionnement biophysique des ondes ultrasonores à l’origine de cette technologie, qui constitue une option non chirurgicale de référence dans la prise en charge de la flaccidité et du relâchement cutané.
Les études présentées ici visent à objectiver les résultats obtenus grâce à cette méthode sur différentes zones du visage : les sourcils, le visage, la région sous-mentonnière et le cou.
Principes de bases de l’action des ultrasons dans un tissu donné
Dès son émission, une onde ultrasonore peut provoquer une perturbation dans un milieu matériel. Dans un milieu biologique non absorbant, une onde ultrasonique provoque des effets mécaniques de type changement de tension, de pression, via sa vélocité agissant ainsi par les biais de forces de cisaillement. Dans un milieu absorbant, cette énergie mécanique se convertit en chaleur engendrant ainsi un effet thermique par l’intermédiaire du phénomène de cavitation. Celui-ci se caractérise par la formation de microbulles au sein du milieu irradié.
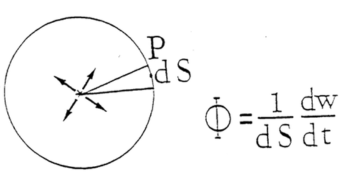
Soit W l’énergie émise par un transducteur ultrasonique sur toute la surface S d’une sphère de rayon R.
dW sera la portion d’énergie reçue par la surface dS située au point P. Cette part d’énergie se calcule par la formule dW = (W/S).dS.
Les effets physiques au point P dépendront donc de la quantité d’énergie dW.dS=W/S et non de l’énergie W totale émise par le transducteur. Ceci explique que l’on tient compte uniquement de la quantité d’énergie par unité de surface. Dans les lignes suivantes, on ne s’intéressera qu’aux mécanismes thermiques des ultrasons. Pour un tissu absorbant, il y aura une génération de chaleur dans l’ensemble du champ de propagation de l’onde progressive ultrasonique.
Si on applique la théorie à l’expérience, on obtient pour une fréquence de 1 MHz et une intensité de 1w/cm2 (intensité d’ordre thérapeutique), une élévation de température de 0.8°C/min. L’augmentation de température est en fait proportionnelle à l’intensité de l’onde ultrasonore ainsi qu’au temps d’exposition du tissu à cette dernière.
Pour information, les pressions de radiation (l’augmentation de la pression induite par l’onde) et les microcourants engendrés ont aussi un effet sur la structure des macromolécules et autres unités biologiques.
Effets thermiques sur le métabolisme
L’effet de l’élévation de la température sur l’activité enzymatique obéit à la règle du Q10 qui spécifie que l’activité enzymatique double pour chaque hausse de 10°C. Si la température du milieu dépasse les 45°C, intervient la dénaturation de ces enzymes diminuant en premier lieu leur activité puis la stoppant définitivement avec les conséquences induites sur le métabolisme et la structure cellulaire (apoptose).
Effets thermiques sur les cellules
Le temps d’exposition à l’onde ultrasonore ainsi que l’élévation de température au sein des tissus déterminent les lésions tissulaires. Les premiers effets au sein d’un tissu absorbant s’observent dès 39 à 43°C sur des périodes d’exposition de l’ordre de la minute. A une température de 44 à 46°C, on observe une coagulation des protéines.
Elévation de température maximale (DTmax) dans les tissus mous et indice thermique (TIS)
Ces deux indices permettent de calculer ainsi la température maximale supportée par un tissu donné et la quantité d’énergie nécessaire pour chauffer le tissu de 1°C. L’indice thermique TIS représente le rapport de l’énergie acoustique moyenne dans le temps de la source (Wo) et de l’énergie acoustique nécessaire à l’élévation de la température du milieu de 1°C (Wdeg):T.I=Wo/Wdeg.
L’indice Wdeg dépend de la fréquence et du coefficient d’absorption du milieu traversé. Pour l’établir, différents modèles de calculs sont utilisés pour estimer la valeur de cet index au niveau des tissus mous. L’indice d’élévation de température animale, quant à lui, est évalué à partir de plusieurs modèles théoriques représentant le milieu en question.
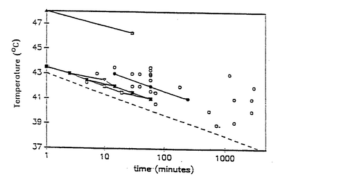
Diagramme température VS temps d’exposition pour l’obtention d’effets biologiques
Chaque point représente soit le temps, soit la température minimum pour l’obtention d’effets biologiques. Les lignes joignent les points correspondant à un même effet biologique. (Miller et Ziskin 1989).
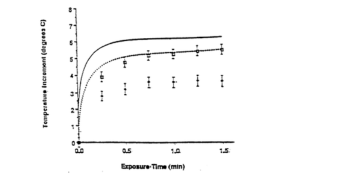
Temps d’exposition entrainant la mort cellulaire en fonction de la température (cellules mammifères normales et tumorales)
On relève que dans cette étude menée sur deux mammifères, le phénomène d’apoptose ne survient chez l’homme et le porc qu’au-delà de 44°.
Application de ces données à la technique HIFU
Petit rappel historique
Ce fut le docteur Franck Fry (1) qui utilisa pour la première fois en 1972 les ultrasons pour détruire des cellules tumorales cérébrales. Près de 30 ans plus tard, en 2004, apparaissent les premières machines mettant en application les ultra-sons à haute intensité dans le traitement facial non invasif avec pour certains d’entre elles une visualisation échographique de la zone traitée. Les premiers essais précliniques sont vite suivis d’essais cliniques essentiellement menés par les docteurs White et Makin (2). Leurs travaux ont permis de valider l’utilisation de l’échographie et ultra-sons focalisés dans le traitement du système musculaire aponévrotique superficiel, pratique devenue courante de nos jours.
Effet biologique de la technique HIFU
La technique du HIFU consiste à concentrer l’énergie des ondes ultrasonores dans la peau, à des zones de profondeurs précises au niveau des fascias superficiels et du derme profond, sans perturber le derme et l’épiderme papillaire. Ces ondes ultrasonores vont opérer un transfert d’énergie acoustique au sein des molécules tissulaires et engendrer une friction et ainsi engendrer des élévations de températures.
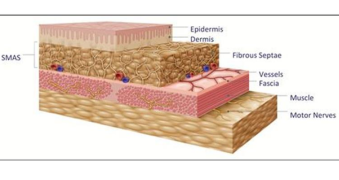
Des points de coagulation thermique (PTC) se forment à des températures avoisinant 60 à 70°C (pour une température en surface de 45 à 47°C), au niveau du derme profond et des couches fibromusculaires, y compris le système aponévrotique musculaire superficiel (SMAS).
Ce processus optimise la néocollagénèse et le remodelage tissulaire, les fibres de collagène dénaturées se contractant, ce qui entraîne un effet de raffermissement de la peau.
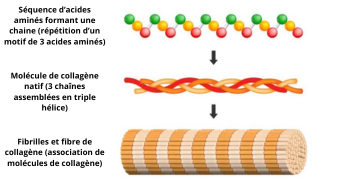
Composition d’une fibre de collagène
Les photos suivantes permettent de comprendre le vieillissement de l’élastine au soleil et seront à comparer à celles plus bas qui illustreront l’effet des HIFU sur ces dernières.
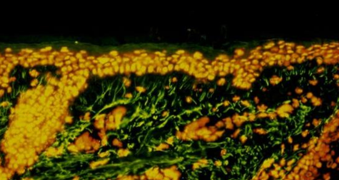
Marquage par immunofluorescence indirecte de l’élastine dans une coupe de peau humaine issue d’une région peu exposée au soleil d’un lifting du visage
L’élastine apparaît en vert et les noyaux des cellules en orange en raison d’une contre coloration à l’iodure de propidium. Dans cette peau issue d’une région peu exposée au soleil, on observe que les fibres élastiques apparaissent sous la forme de fines fibrilles.
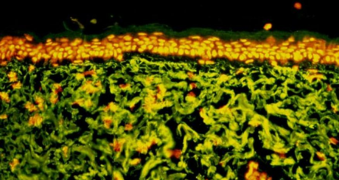
Marquage par immunofluorescence indirecte de l’élastine dans une coupe de peau humaine issue d’une région exposée au soleil d’un lifting du visage
Dans cette peau issue d’une région exposée au soleil, on observe que les fibres élastiques apparaissent sous la forme d’amas de matériel élastotique caractéristique d’une peau photo vieillie.
Le propre de la technique HIFU est de chauffer une zone précise de tissu sans pour autant affecter les autres tissus dans son champ de propagation. La forme concave de la sonde ultrasonore permet, par effet de loupe, de concentrer l’énergie acoustique sur des zones tissulaires de profondeur très ciblée (1.5 mm – couche cutanée superficielle – 3 mm et 4.5 mm (SMAS)). Cette élévation localisée de température entraîne une mort cellulaire contrôlée, accompagnée de phénomènes inflammatoires associés, tout en préservant les tissus environnants de tout effet cytotoxique. Ces effets se manifestent dans les zones ciblées, en fonction de la spécificité de la sonde utilisée.
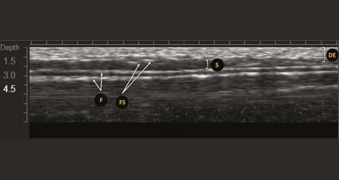
Image échographique obtenue avec un transducteur MFU-V. Le derme et l’épiderme (DE), le fascia (F), les septaes fibreuses (FS) et les adipeux sous-cutanés (SA) sont représentés.
Les effets de ces points de coagulations thermiques peuvent se diviser en trois phases :
- De manière très précoce (1 à 3 jours), apparait la production des médiateurs de type interleukines (IL1 et IL6 notamment), cytokines principales de l’inflammation. Le necrosis tumoral factor, le TNF-alpha permet le recrutement de lymphocytes et de polynucléaires neutrophiles, participant ainsi au remodelage et à la réparation des tissus lésés. D’autres facteurs non moins importants tels que le FGF-2, facteur de croissance des fibroblastes; l’IGF1 (facteur de croissance insulinique) luttant contre le stress oxydant; le TGF-beta (facteur de croissance transformant) jouant un rôle prépondérant dans le développement tissulaire et le VGEF (facteur de croissance de l’endothélium vasculaire) permettant l’angiogenèse nécessaire à la croissance des néo tissus : l’ensemble de ces facteurs précoces amène la production de collagène et d’élastine ainsi que la néovascularisation au sein de la matrice extracellulaire.
- La seconde phase, plus tardive (entre 5 et 10 jours), correspond à l’activation des fibroblastes, qui synthétisent les substances nécessaires à la cicatrisation des tissus, telles que le collagène et la fibronectine. Ce processus est régulé par les cytokines IFN-alpha et TGF-beta mentionnés ci-dessus, permettant ainsi la création d’une nouvelle matrice de tissu conjonctif, destinée à combler les lacunes et à restaurer la résistance mécanique des tissus.
- La dernière phase, qui peut s’étendre du 21ème jour jusqu’à près d’un an, correspond à la synthèse de collagène en remplacement des tissus lésés, tandis que la prolifération des fibroblastes diminue progressivement.
De manière synthétique, il est facile de comprendre l’importance de la phase précoce d’action tissulaire des HIFU, au cours de laquelle les facteurs de stimulation des fibroblastes induisent la synthèse des deux molécules principales impliquées dans la régénération cutanée : le collagène et l’élastine. Ce mécanisme constitue la base du processus de réparation des plaies chez les mammifères.

Evaluation anatomopathologique des HIFU
La pénétration des ondes HIFU et la profondeur d’injection dépendent de l’état du système aponévrotique musculaire superficiel (SMAS) et du système de fascia superficiel (SFS), en fonction de l’effet recherché (lifting ou raffermissement).
En effet, le nombre de points de coagulation thermique (PTC) déterminera le niveau de resserrement suffisant pour raffermir la peau. L’idéal est de cibler précisément la profondeur de ces zones, ce qui conditionne le choix des transducteurs (1.5 mm, 3 mm ou 4.5 mm), à partir d’une visualisation préalable des structures anatomiques concernées. Or, le SMAS et le SFS varient selon l’âge, le sexe et l’IMC (3).
Le nombre de lignes nécessaires à un effet tonifiant dépend alors du transducteur utilisé et de la surface de couverture qu’il fournit. Cela doit être pris en compte en fonction de l’aspect esthétique initial, de la gravité de la flaccidité du muscle platysma et des objectifs définis avec le patient. En effet, plus la couverture linéaire et la densité des lignes sont importantes dans la zone du cou, plus la production de libres de collagène et d’élastine sera significative, comme le montre l’étude du Dr Sasaki et al. (4).
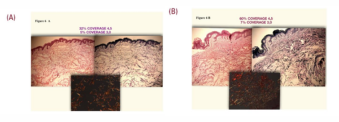
Peau traitée après une couverture HIFU de 32% avec 4.5 mm de profondeur et de 5% à 3 mm de profondeur (photo A) et 60% à 4.5 mm et 7% à 3 mm (photo B)
Le colorant utilisé met en évidence une densité et une quantité plus importantes de fibres de collagène sur la photo B, où le nombre de lignes de traitement et la couverture de la zone traitée sont plus élevés.