Conflit d’intérêt
Ce travail n’a bénéficié d’aucun support, tant financier que matériel. Il est le résultat d’une recherche, d’un travail et d’un financement strictement personnel et n’engage que l’auteur principal (PM).
P Micheels est consultant et/ou formateur pour les laboratoires Allergan, Galderma, Merz, Teoxane.
Introduction
Depuis 1994-1995, soit plus de 20 ans aujourd’hui (Ref 1, 2), les gels d’acide hyaluronique (HA) ont pris le pas sur la plupart des produits de comblement de rides. Ceci est la conséquence de la nature sans spécificité d’espèce ou d’organe de la forme native de l’HA, et du peu d’effets secondaires observés ou mieux, déclarés. On peut, en effet, supposer que le taux annoncé par la littérature est supérieur dans la réalité. (Ref 3 – 6)
En effet, une fois réticulé, l’HA n’est plus du tout un produit naturel, ne serait-ce que par sa structure tri-dimensionnelle dans l’espace. Il peut donc être reconnu comme un corps étranger par notre organisme et plus spécifiquement par notre derme, lieu des défenses immunitaires de notre peau. (Ref 6)
Aujourd’hui, sur le marché européen, il existe un grand nombre de gels d’HA à disposition. Ils ont tous des caractéristiques différentes, dues à leur processus de réticulation, souvent breveté et protégé.
Il faut noter que lorsque nous injectons un gel d’HA, que ce soit dans le derme ou en sus-périosté, voire dans la graisse, le gel subit diverses contraintes physiques.
Dans cet article, nous examinons 10 gels d’HA, dont 3 sont, déjà, au bénéfice d’une approbation par la FDA (Food and Drugs Administration) aux Etats-Unis d’Amérique.
7 des 10 gels examinés sont additionnés de lidocaïne dès leur fabrication. Les 10 gels testés ont les mêmes indications, à savoir combler les rides et plis moyens du visage, et pour certains, l’ourlet de lèvres, voire l’augmentation ou la correction de la volumétrie du visage et des lèvres.
Le but de ce travail est de vérifier si notre ressenti personnel, à l’opposé des assertions des délégués médicaux, voire des fabricants eux-mêmes, dès l’apparition de ces gels additionnés de lidocaïne, correspondait bien à la réalité. (Ref 4)
Nous avons donc, par comparaison, examiné également 3 de ces gels, non additionnés de lidocaïne.
Les tests réalisés sont des tests de rhéologie sous différentes contraintes mécaniques
Matériel
Les gels examinés
10 gels, tous réticulés avec le BDDE (Butane Diol Diglycidyl Ether) et ayant les mêmes indications d’utilisation sont l’objet de ce travail. Ils s’injectent dans le derme moyen à profond, pour combler les rides et les plis moyens. Certains, cependant, peuvent être injectés dans le derme superficiel. (Ref 7-11)
Nous les avons classés suivant leur nature, dite cohésive, non cohésive ou partiellement cohésive, suivant les données de la littérature. (Ref 12 -17, et communication personnelle de Dr Albarano –Galderma fév 2016)

Si l’ajout de lidocaïne ne semble pas modifier la structure ultramicroscopique des gels d’HA (Ref 12-17), dans notre pratique quotidienne (PM), il nous a semblé que certains gels additionnés de lidocaïne étaient moins aisément injectables, moins fluides, que leur alter-ego exempts de lidocaïne. Ce ressenti était déjà présent lors d’une étude multicentrique européenne, dont PM a fait partie, lors de la commercialisation d’un gel partiellement cohésif lidocaïné. (Ref 3, 4)
Afin de vérifier notre assertion concernant l’adjonction de lidocaïne, à savoir qu’elle modifiait ou non les propriétés rhéologiques des gels, nous avons pratiqué les mêmes tests sur les produits suivants :
 Les gels ont été testés avec un rhéomètre DHR III (TA Instrument). Les mesures ont été réalisées à l’aide d’une géométrie plan-plan rugueux de 25mm de diamètre, la température régulée par un plan à effet Peltier. Chaque test a été effectué au moins 2 fois, sur des échantillons différents, pour évaluer la reproductibilité (voir écart-type dans les tableaux ci-dessous).
Les gels ont été testés avec un rhéomètre DHR III (TA Instrument). Les mesures ont été réalisées à l’aide d’une géométrie plan-plan rugueux de 25mm de diamètre, la température régulée par un plan à effet Peltier. Chaque test a été effectué au moins 2 fois, sur des échantillons différents, pour évaluer la reproductibilité (voir écart-type dans les tableaux ci-dessous).
Méthode
Avant toute mesure, l’échantillon est déposé sur le plan inférieur puis étalé à l’aide du plan supérieur. Le surplus de produit est enlevé à la spatule. L’entrefer est ensuite réglé et l’échantillon conditionné à la température de mesure (25°C) avec une précision de 0.5°C.
Les différents tests sont :
- balayage en déformation (strain sweep) de 0.01 à 3000%, fréquence 1Hz, pour dégager les modules élastique, visqueux et tangente delta -tan(δ) – au plateau, ainsi que les valeurs de déformation, de contrainte et de module au point de cross-over. Les valeurs d’aire sous la courbe d’évolution du module élastique G’ en fonction de la contrainte appliquée seront également relevées. Rappelons que pour ces mesures, le gel subit une pression constante, avec une oscillation stable à 1Hz, toujours de même amplitude. On mesure donc comment le gel répond à cette contrainte et suit l’oscillation sinusoïdale imposée
- Des balayages en fréquence (frequency sweep) de 0.1 à 100Hz pour dégager les valeurs des modules élastiques G’ et visqueux G’’ sous une déformation faisant partie du domaine linéaire.
Rappels
Domaine linéaire de visco-élasticité : représente la zone dans laquelle la valeur des modules viscoélastiques (G’etG’’) ne dépend pas de la contrainte ou de la déformation appliquée.
G’ : représente la composante /contribution élastique du module complexe en cisaillement.
G’’ : représente la composante /contribution visqueuse du module complexe en cisaillement.
Tan δ (Tangente delta): est le rapport G’’ sur G’ (G’’/G’). Cette donnée caractérise la viscoélasticité du produit.
Si ce rapport est proche de 0, le fluide est élastique, proche d’un solide. Plus le rapport est proche de 1, plus le fluide est visqueux, moins sa composante élastique est importante.
Stress (contrainte) : représente la contrainte appliquée au gel. Elle s’exprime en Pascal (Pa). En théorie, plus la valeur de la contrainte est grande au point de cross-over, plus le gel serait difficile à
injecter.
Strain (Déformation) : Déformation du gel. Elle s’exprime en %. Plus la valeur de la déformation au point de
cross-over est élevée, plus le gel serait susceptible de durer dans le temps.
Point de cross-over : représente le moment où les courbes G’ et G’’ se croisent. C’est aussi le point d’écoulement.
En théorie, plus la valeur de contrainte au point de cross-over est grande, plus le produit
sera difficile à injecter. De même, plus la valeur de déformation au point de cross-over est
élevée, plus le produit serait, théoriquement, susceptible de perdurer.
G’=G’’ : C’est le point de cross-over mentionné plus haut. A ce point, la viscosité est égale à l’élasticité.
Résultats
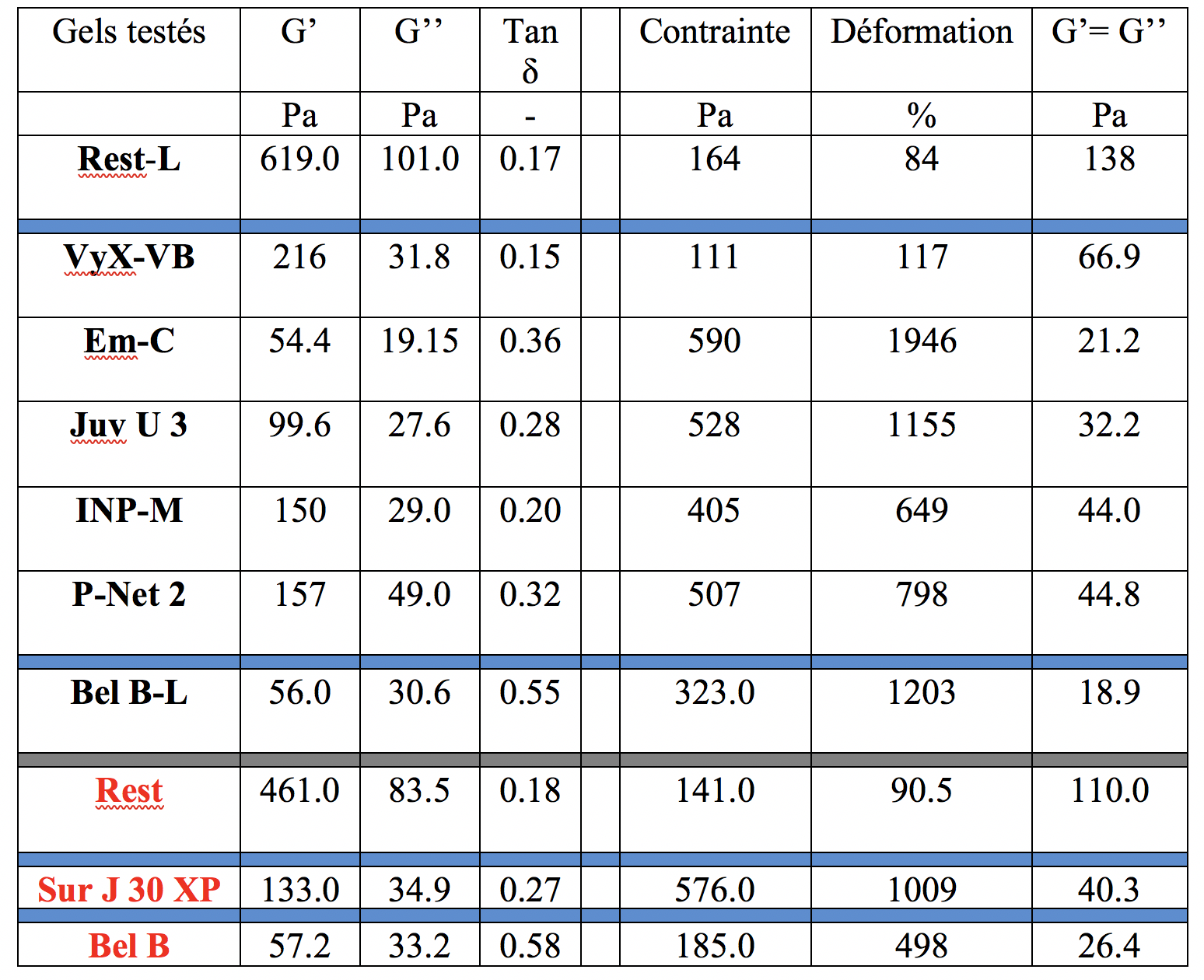
Le tableau 1 reprend l’ensemble des résultats obtenus sur les différents gels d’HA testés.
Nous allons d’abord étudier les résultats des 3 gels pour lesquels nous avons un comparatif avec et sans lidocaïne. Ensuite nous donnerons quelques commentaires sur l’ensemble des tests réalisés sur les autres gels d’HA de cette étude.
Comparaison des 3 gels FDA
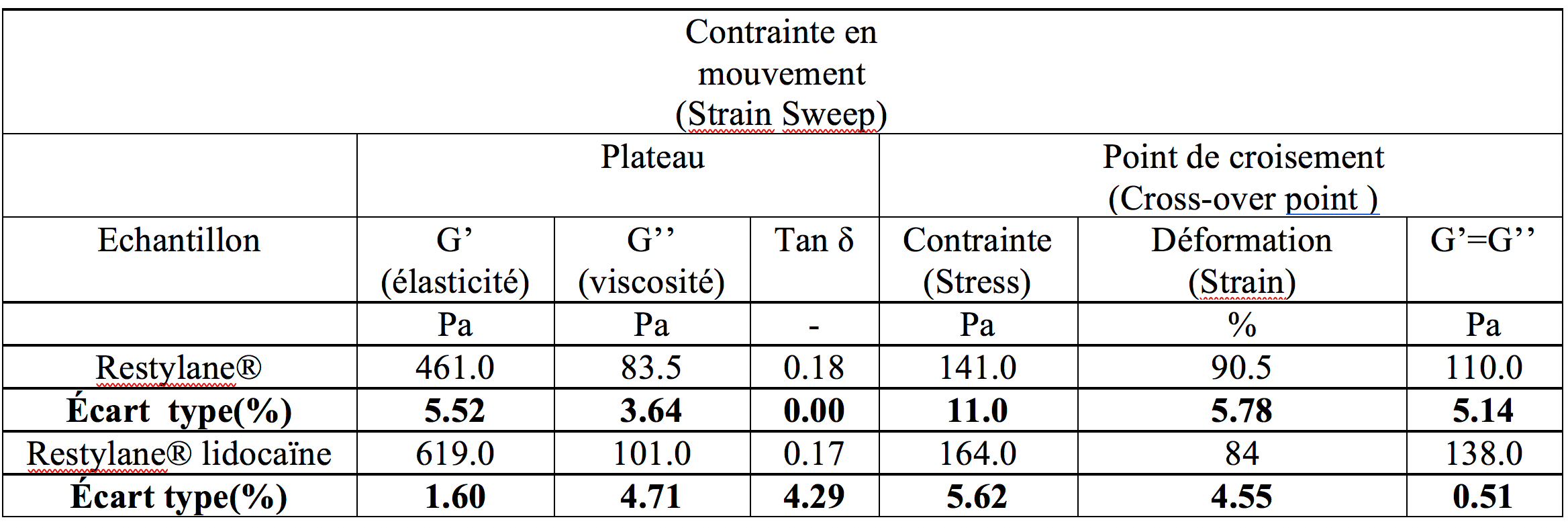
On constate que les gels NASHA® Restylane® avec et sans lidocaïne possèdent des caractéristiques viscoélastiques proches car leur Tan δ sont très similaires.
On constate néanmoins que le module élastique G’ du produit Restylane® avec lidocaïne est significativement supérieur à celui du produit sans lidocaïne.
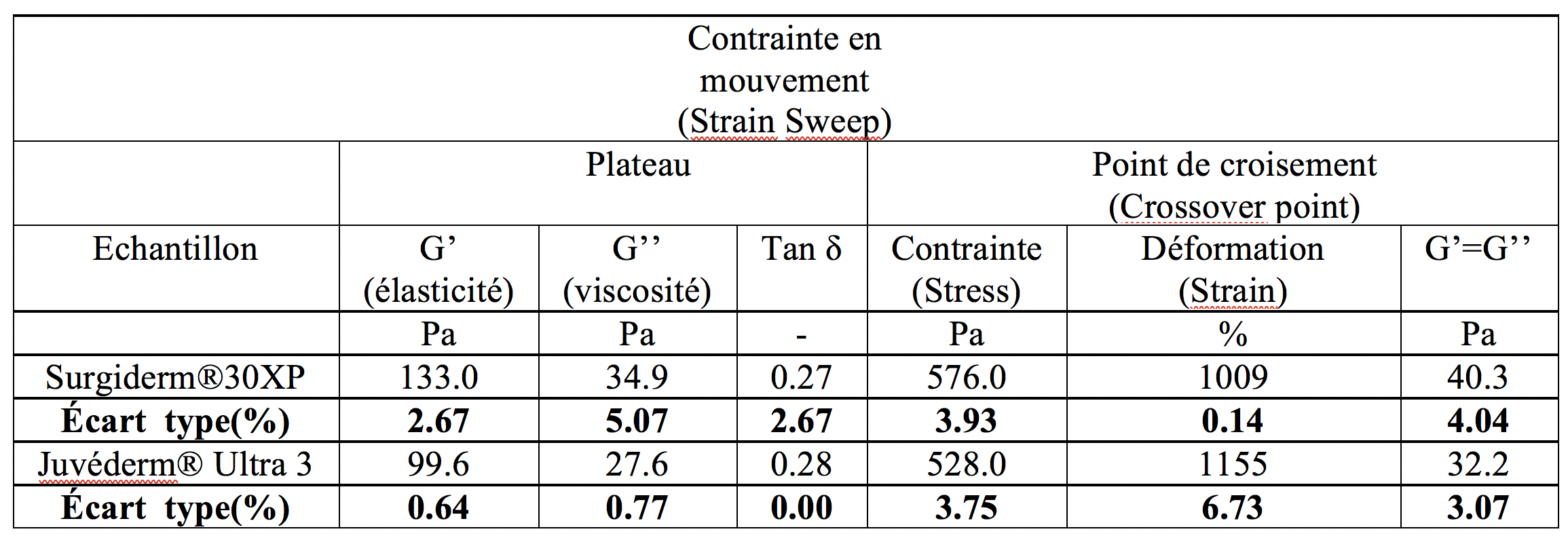
On constate que les gels Surgiderm® 30XP sans lidocaïne et Juvéderm® Ultra 3avec lidocaïne possèdent des caractéristiques viscoélastiques proches car leur Tan δ sont ici aussi très similaires.
Néanmoins le module élastique G’ du produit Surgiderm® 30XP est significativement supérieur à celui du produit Juvéderm® Ultra 3.
Comparés aux gels de références que sont les gels NASHA®, ces 2 gels partiellement cohésifs sont moins élastiques (tan δ plus élevé et G’ plus faible).
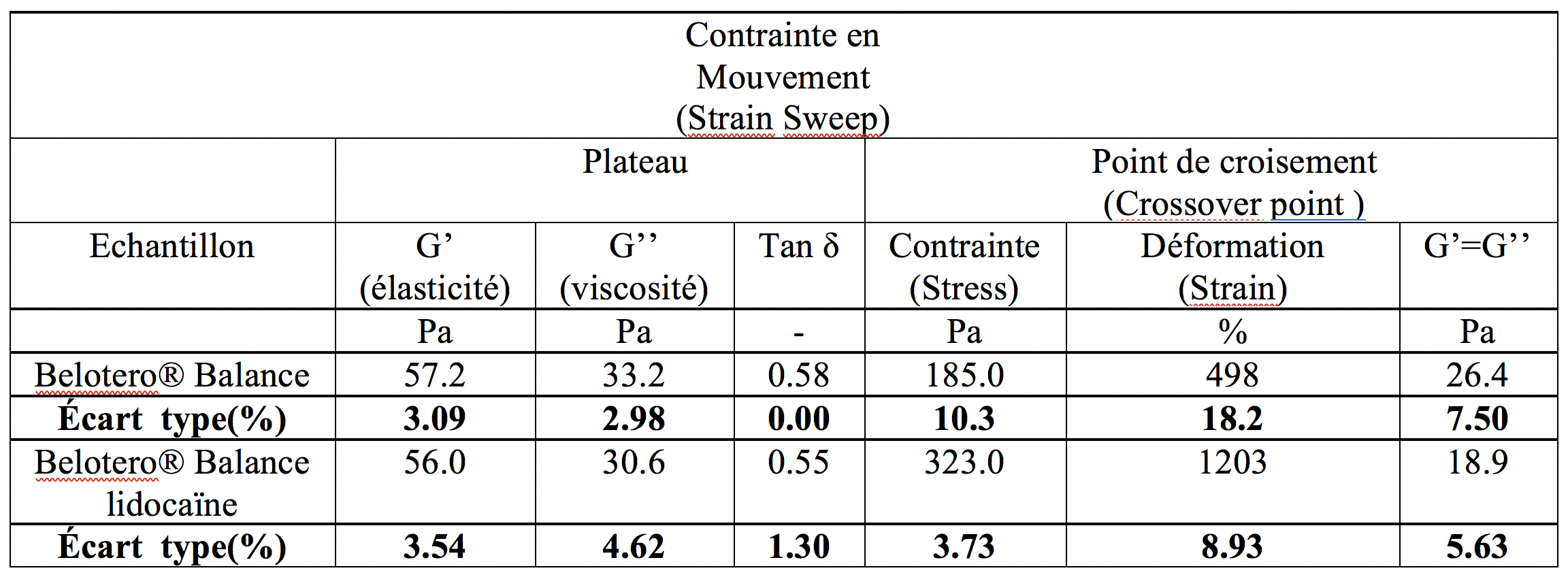
Les modules d’élasticité et de viscosité de ces 2 préparations, sont très semblables, avec un tan δ un peu plus élevé pour le produit sans lidocaïne, dont peut-être un peu plus visqueux, moins élastique, plus éloigné d’un solide…ce qui est en concordance avec le ressenti de l’auteur (PM).
Au point de cross-over, les valeurs en déformation et en contrainte ne sont plus semblables. On observe une augmentation de 74.6% de la valeur en contrainte, et 142% pour celle en déformation pour le gel avec lidocaïne. Ce gel est le plus modifié par l’adjonction de la lidocaïne. CPM® Lido serait donc plus difficile à injecter, en concordance avec le ressenti de l’auteur (PM), et serait de plus longue tenue dans le temps que sa formulation exempte de lidocaïne. Ceci serait à contrôler par une étude comparative.
On observe donc une évidente différence de comportement du gel CPM® avec ou sans lidocaïne.
Commentaires sur les gels testés
Avant tout commentaire sur les gels d’HA testés dans cette étude, nous aimerions apporter ce qui suit. La chaleur est un des facteurs de dégradation de l’HA. La lidocaïne, lors de son ajout au cours de la fabrication des gels d’HA semble entourer les fibres d’HA, à la manière d’un manteau. De ce fait, elle pourrait entraîner des modifications des propriétés rhéologiques des gels d’HA et rendre le gel plus résistant à la dégradation par la chaleur, par exemple lors de la stérilisation. Les gels pourraient donc être plus visqueux à la fin du processus de fabrication.
Gel non cohésif avec et sans lidocaïne
Rest-L
Les valeurs de contrainte au point de cross-over de Restylane® lidocaïne sont légèrement supérieures au gel sans lidocaïne. Il serait donc, dans l’absolu, légèrement plus difficile à injecter et d’une tenue dans le temps un peu plus longue que son alter ego sans lidocaïne. Cependant en pratique, PM n’a jamais eu ce ressenti.
Les valeurs en déformation au point de cross-over sont, elles, légèrement inférieures au gel sans lidocaïne.
Restylane® sans lidocaïne serait légèrement plus difficile à injecter, et serait, en théorie, susceptible de tenir très légèrement moins dans le temps que sa formule avec lidocaïne. Ceci demanderait une étude comparative.
Il existe donc une discordance entre les valeurs de contrainte et en déformation au point de cross-over pour ces deux gels non cohésifs.
On peut considérer que les 2 gels NASHA®, avec ou sans lidocaïne, sont comparables, quant à leurs propriétés rhéologiques. L’addition de lidocaïne n’a pas ou peu modifié le gel.
Suivant le fabricant, les données rhéologiques des 2 gels seraient très semblables (communication personnelle
Par mail Dr T. Albarano-Galderma, 10.06.2016)
Gels partiellement cohésifs avec et sans lidocaïne
Nous séparons ici les gels d’HA pour lesquels nous avons un comparatif sans lidocaïne (Allergan). Nous y joignons le gel de nouvelle génération de ce fabricant. Ceci nous permet de faire un comparatif entre ces 3 gels, présentant les mêmes indications de traitement.
SurJ 30 et Juv U 3
SurJ 30 et Juv U 3 ont des valeurs très proches. On peut donc les considérer comme équivalents. Ceci semble contredire les impressions personnelles de l’injecteur (PM). Sauf si, entre la mise sur le marché de Juvéderm® Ultra 3 et les seringues actuellement sur le marché, une amélioration du contrôle des qualités rhéologiques du produit a été apportée. Il serait donc intéressant de faire les mêmes mesures avec les gels de 2007-2008.
VyX-VB
Ce gel, de technologie de réticulation Vycross®, présente des caractéristiques rhéologiques totalement différentes de ses 2 prédécesseurs.
En effet, la technologie de réticulation de ce produit n’est pas identique à SurJ 30 et Juv U 3 (Matrice 3 D® et Vycross®), ne serait-ce que par l’inversion des proportions entre les fibres de haute et faible masse moléculaire.
Le module élastique (G’) de VyX-VB est plus élevé que les autres gels d’Allergan, se rapprochant, très grossièrement, des valeurs des gels NASHA®.
Ceci pourrait signifier que VyX-VB, de par sa technologie spécifique de réticulation, par rapport à Juv U 3 et SurJ 30, entraîne une réticulation plus efficace, ce qui est revendiqué par le laboratoire, un maillage plus compact, donc, plus résistant aux forces de cisaillement, plus proche d’un solide, toute proportion gardée, cela va sans dire !
Ce gel présente un rapport G’’/G’ (Tan δ) le plus faible de tous les gels testés. Ses propriétés sont donc plus élastiques que ses prédécesseurs. Ce gel présenterait donc des propriétés proches de NASHA®.
En termes de contrainte au point de cross-over, le produit Volbella® présente une diminution de 79.80%, comparé aux deux autres gels d’HA testés du laboratoire Allergan, ainsi qu’une diminution de 89.20% de la valeur de déformation, toujours au point de cross-over.
La valeur de la contrainte au point de cross-over étant très basse, cela voudrait dire que le gel est très aisé à injecter. C’est ce que l’on observe en pratique.
Par contre, rhéologiquement et théoriquement, la valeur de la déformation au point de cross-over, étant basse, pourrait laisser penser que la tenue dans le temps du gel Volbella® pourrait être inférieure à Juv U 3 et SurJ 30. Ceci n’est cependant pas ce que l’on observe en pratique, mais resterait, quand même à démontrer, par une étude comparative.
Toujours dans ce paragraphe concernant les gels partiellement cohésifs, nous donnons les valeurs que nous avons obtenues pour 3 autres gels d’HA présents du marché européen, et qui ont, eux aussi, les mêmes indications que tous les gels d’HA de cette étude.
Em-C
Le gel au bénéfice de la technique de réticulation « Optimal Balance Technology® » présente des valeurs de contrainte et de déformation au point de cross-over supérieures aux 2 autres gels présentés dans ce paragraphe (INP-M et P-Net 2). Il serait donc plus difficile à injecter, mais présenterait une rémanence possiblement supérieure.
Ceci reste à démontrer.
INP-M
Ce gel présente des modules d’élasticité et de viscosité comparables aux autres gels partiellement cohésifs. Il en est de même pour les valeurs au point de cross-over, tant pour la contrainte que pour la déformation, à l’exception du gel VyX-VB.
P-Net 2 (RHA® 2)
On peut considérer ce gel comme présentant des valeurs proches de ses concurrents partiellement cohésifs, à l’exception toujours du gel VyX-VB.
Gel cohésif avec et sans lidocaïne
L’ajout de lidocaïne au gel CPM® engendre, contrairement à certaines assertions, de grandes modifications des propriétés rhéologiques, comparé au gel original sans lidocaïne.
Certes, les mesures G’ et G’’, ainsi que Tan δ sont très semblables pour les 2 préparations. Ceci signifie une bonne maitrise du contrôle des propriétés viscoélastiques du gel.
Cependant, pour le gel CPM® avec lidocaïne, les valeurs de contrainte au point de cross-over sont supérieures de 74.60% et celles pour la déformation, toujours au point de cross-over, le sont de 142.00%, comparativement au gel sans lidocaïne.
Il existe donc bel et bien une nette différence entre le gel additionné ou non de lidocaïne.
Ceci signifie, en théorie, que CPM® Lido serait plus difficile à injecter-ceci correspond parfaitement au ressenti de PM- et serait de plus longue tenue dans le temps que sa formule sans lidocaïne. Ceci nécessiterait comme pour d’autres gels de ce travail, une étude comparative. (Ref 16, 17)
Discussion
Les résultats obtenus, dans cette étude, sont, dans l’ensemble, reproductibles. Deux produits se démarquent aux valeurs de contrainte et de déformation au point de cross-over.
Ces deux gels présentent des caractéristiques totalement opposées, du fait de leur technologie de réticulation, l’une menant à un gel totalement non cohésif (NASHA®) et l’autre à un gel totalement cohésif (CPM®).
Les autres gels sont classifiables comme partiellement cohésifs et présentent des valeurs intermédiaires par rapport aux 2 premiers. (Ref 13, 14)
1. Le gel CPM®
L’ajout de lidocaïne au gel CPM® entraîne une augmentation de 74.60% pour la contrainte et de 142.00% pour la déformation. Ces deux gels sont donc différents en termes de rhéologie. L’ajout de lidocaïne a rendu Belotero® plus visqueux, plus difficile à injecter. Ces analyses confirment donc l’impression clinique de PM, ressentie depuis sa mise sur le marché.
Ces propriétés devraient entrainer une tenue dans le temps supérieure à celle du produit sans lidocaïne. Ceci nécessite une étude comparative, pour vérifier cette assertion.
2. Le gel NASHA®
Pour le gel NASHA®, l’ajout de lidocaïne à la préparation entraine, elle aussi, une augmentation des valeurs de contrainte de 16.30%. Par contre, nous observons, en déformation, une baisse des valeurs de 7.18%. Le gel NASHA® lidocaïne devrait donc être plus fluide, plus facile à injecter que son équivalent sans lidocaïne.
Il est difficile de donner un avis sur ce point, les différences étant très faibles et probablement difficilement ressenties par des mains, même expertes.
3. Au sein de la gamme des produits Allergan
Il existe des variations entre la formule Matrice 3D® avec et sans lidocaïne. En effet, lors de la mise sur le marché de la gamme Matrice 3D® avec lidocaïne, à savoir Juvéderm® Ultra 3, ce dernier nous a été présenté, par le laboratoire Allergan lui-même, comme son prédécesseur (Surgiderm®30XP) additionné de lidocaïne, avec strictement les mêmes propriétés d’injectabilité.
Nous avons, lors de l’étude post marketing de Wahl (Ref 3, 4), immédiatement notifié, avec entretien, à l’époque, avec le Dr. K. Tan (Allergan), que notre impression était toute autre, et que nous n’avions pas du tout le même ressenti lors de l’injection de ce gel lidocaïné, comparé à nos traitements avec le gel sans lidocaïne. Le gel lidocaïné nous semblait nettement plus visqueux, en tout cas à l’époque.
Il semble ressortir, ici, de cette étude comparative des propriétés rhéologiques des gels d’HA additionné ou non de lidocaïne que le gel Juvéderm® Ultra 3 présente des valeurs, malgré nos impressions cliniques, assez proches de celles de Surgiderm® 30 XP.
Cependant, la valeur de contrainte au cross-over (strain) de Juvéderm® Ultra 3 étant supérieure à celle de Surgiderm®30XP, on pourrait ressentir une plus forte résistance à l’injection de Juvéderm® Ultra 3. Ceci correspond bien au ressenti de PM lors des traitements de comblement des rides dans sa pratique quotidienne.
Le gel Volbella®, lui, est totalement différent. Il présente une diminution de contrainte au cross-over de 79.80% et pour la déformation au cross-over de 89.20%. Ce gel est donc particulièrement aisé à injecter, ce qui correspond bien à la pratique quotidienne et aux « revendications » du fabricant.
4. Pour les autres gels partiellement cohésifs testés
Pour les gels « Inter Penetrating Network-like » (Stylage® M), ainsi que pour « Optimal Balance technology » (Emervel® Classic), nous n’avons pas de comparatifs avec un gel de même facture sans lidocaïne.
La caractérisation rhéologique des gels d’acide hyaluronique « Preserved Network » (RHA® 2) est connue (Laboratoires Teoxane. Données internes). Nous n’avons pas de comparatifs face à un gel de même facture sans lidocaïne. Les données internes et les nôtres sont superposables.
Conclusion
De tous les tests pratiqués que nous avons fait faire en milieu indépendant, il ressort que l’ajout de lidocaïne aux gels d’HA, pour lesquels nous avons le correspondant sans addition de lidocaïne, en change, plus ou moins de manière significative, les propriétés rhéologiques.
Plus la valeur de contrainte au pointde cross-over est élevée, plus les gels avec lidocaïne semblent plus difficiles à injecter.
Il se pourrait aussi que les gels d’HA, présentant une valeur de la déformation au point de cross-over élevée, puissent avoir une rémanence supérieure aux gels d’HA sans lidocaïne.
Il faudrait compléter cette étude par une étude comparant les résultats observés en pratique et les confronter avec les résultats et interprétation des données théoriques de cette étude-ci.
Ceci permettrait de prouver que les gels présentant de fortes valeurs de contrainte au point de cross-over sont ou non systématiquement plus difficiles à injecter. Cette étude permettrait aussi de prouver la relation entre augmentation de la contrainte au point de cross-over et ajout de lidocaïne.
Tableau 1 : Résultats des tests de rhéologie réalisés au laboratoire Rheonova-France. En noir les gels avec lidocaïne, en rouge les gels de référence, sans lidocaïne. Nous avons séparé les gels non cohésifs, partiellement cohésifs et totalement cohésifs, suivant la classification de Sundaram et al. (Ref 13)
Références
- Olenius M.: “The first clinical study using a new biodegradable implant for the treatment of lips, wrinkles and
folds. Aesth. Plast.Surg 1998; 22 : 97-101. - Piaquadio D., Jarko M., Goltz R.: “Evaluation of hylan B gel for soft tissue augmentation implant material.” J Am Acad Dermatol 1997; 36 : 544-549.
- Ballin A. C., Cazzaniga A., Brandt F.S. : « Long-term efficacy, safety and durability of Juvéderm® XP. » Clinical, Cosmetic and Investigational Dermatology. 2013 ;6 :183-189.
- Wahl G. : « European evaluation of a new hyaluronic acid filler incorporating lidocaine. » J. Cosmet Dermatol. 2008 ;7 :298-303.
- Artzi O, Loizides C, Verner I, Landau M. : « Resistant and recurrent late reaction to hyaluronic acid-based gel. » Dermatol Surg. 2016;42:3137.
- Micheels P. : « Human Anti-Hyaluronic Acid Antibodies : is it possible ? ». Dermatol Surg. 2001 ; 27 :185-191.
- Allergan : use leaflet Surgiderm® 30 XP, Juvéderm® Ultra 3 and Volbella®.
- Merz : use leaflet Belotero® Balance with and without lidocaine.
- Q-Med-Galderma : use leaflet Restylane®, Restylane® with lidocain, and Emervel® Classic.
- Teoxane : use leaflet RHA®2 with lidocaine.
- Vivacy : use leaflet Stylage® M.
- Flynn T.C., Thompson D. Hyun S-H., Howell D. : « Ultrastructural analysis of 3 hyaluronic acid soft-tissue fillers using scanning electron microscopy. » Dermatol. Surg. 2015 ; 41 : S143-S152.
- Sundaram H., Rohrich R, Liew St et al : « Cohesivity of hyaluronic acid fillers : development and clinical implications of a novel essay, pilot validation with a five-point grading scale, and evaluation of 6 U.S. Food and Drug administration-approved fillers. » PRS Journal.com 2015.
- Gavard Molliard S., Albert S., Mondon K.: « Key importance of compression properties in the biophysical characteristics of hyaluronic acid soft-tissues fillers. » J. Mech.Behavior of Biomaterials 2016 ; 61 : 290-298
- Mondon K., Dadras M., Tillier J., Gavard Molliard S. : « Influence of the macro-and/or microstructure of crosslinked hyaluronic acid hydrogels on the release of two model drugs. » J. Glycobiology 2016 ; 5 :1 ISSN :2168-958X JGB, open access journal.
- Micheels P., Besse.S ; Sarazin D., Obamba M. : »Hyaluronic acid gel based on CPM® technology with and without lidocaine: Is there a difference? » JDD. En cours de publication.
- W. Prager, P. Micheels : «A prospective, comparative survey to investigate practitioners’ satisfaction with a cohesive, polydensified-matrix®, hyaluronic acid-based filler gel with and without lidocaine for the treatment of facial wrinkles. » Journal of Cosmetic Dermatology December 2014.
-
Note du comité de lecture




4 commentaires
Bonjour dicteur
Mon médecin esthétique jusqu’à maintenant m’injectait du Restylane chez Galderma, mais vient de me faire une injection sans me prévenir de Révolax. Que pensez-vous de cette acide hyaluronique ?
Merci de votre réponse
Merci pour cette recherche poussée sur le sujet. J’apprécie beaucoup votre déclaration quant au conflit d’intérêt qui est susceptible de survenir dans de tels travaux. Je serais curieux en effet de voir des études pratiques sur les différents acides hyaluroniques.
moi je suis alergique a la lidocaine .
je cherche un acide hyaluronique sans lidocaine comme il y avait avant.
Car je ne peu plus en bénificier maintenant.
Il existe toujours des versions d’acide hyaluronique sans lidocaïne. Le médecin peut s’en procurer si vous lui demandez.