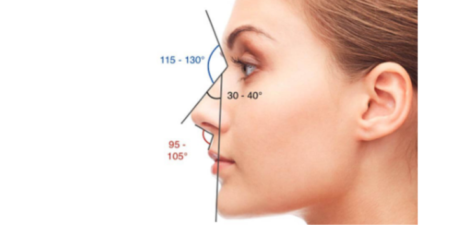
L’acide hyaluronique (HA) est, depuis 20 ans, devenu progressivement le produit de référence pour le comblement des rides et la volumétrie du visage. (Réf 1, 2)
Le marché étant très porteur, c’est l’une des principales demandes de traitement esthétique tant aux Etats-Unis d’Amérique qu’en Europe ou Orient. Il existe donc de très nombreux laboratoires fabriquant des gels d’HA pour les traitements à visée esthétique.
Certains gels sont depuis plusieurs années acceptés par la Food and Drug Administration (FDA) aux Etats Unis.
D’autres sont en cours d’enregistrement. C’est un de ces derniers que nous allons présenter ici.
Nous avons choisi un gel d’AH fabriqué en Suisse, à Genève. Il existe au sein de la société fabricante 2 familles de gels de comblement de rides, qui peuvent prêter à confusion, raison princeps de cet article. Cet article est aussi un complément à un article précédemment publié en français, tant dans le Journal de Médecine Esthétique et Chirurgie Dermatologique, ou dans DermActu, qu’en anglais, dans Journal of Drugs in Dermatology. (Réf 3, 4, 5)
A la demande du Dr P. Micheels, le laboratoire Teoxane – Geneva, Switzerland, a sponsorisé exclusivement le travail sur le produit Teosyal® RHA 2.
Matériel
A. Les gels examinés
A.1 Teosyal® PureSense Global Action
Lors d’une précédente étude comparative (Réf 3, 4, 5), nous avons examiné le gel :
- Teosyal® PureSense Global Action, Laboratoire Teoxane-Genève, Suisse- lot n° TS30L134103C5926 Exp: 2015.10.
Ce gel est réticulé avec du butane diol diglycidyl ether (BDDE).
La technologie brevetée des gels Teosyal® est basée sur la réticulation en une étape, d’acide hyaluronique de grade pharmaceutique, de haute masse moléculaire, au sein d’une poche déformable stérile. Les gels obtenus se caractérisent par un réseau de réticulation homogène (distribution isotrope des ponts de réticulation), leur conférant des propriétés d’élasticité et de cohésivité équilibrées (index de cohésivité mesuré par rhéologie en compression).
(Communication personnelle Mr Meunier-Laboratoires Teoxane)
Ses indications sont :
- le comblement des rides et plis fins à moyens.
A.2 Teosyal® RHA Preserved Network
Les gels commercialisés sous la dénomination Teosyal® RHA (Resilient Hyaluronic Acid) 1, 2, 3, 4, actuellement en cours d’approbation par la FDA (communication personnelle de Mr Meunier-laboratoires Teoxane-Genève, Suisse) relèvent de la technologie dite « Preserved Network », résultant de l’optimisation de la méthode de réticulation des gels Teosyal®.
La technologie « Preserved Network » permet d’optimiser la protection des chaînes d’acide hyaluronique de haut poids moléculaire afin de minimiser leur dégradation lors de l’étape de réticulation. Par ce moyen, dans le gel réticulé, les interactions mobiles naturelles entre les chaînes d’acide hyaluronique sont préservées, et la quantité d’agent réticulant est réduite.
En plus de propriétés d’élasticité et de cohésivité au moins équivalentes au gel Teosyal® Pure Sense, les gels Teosyal® RHA présentent des propriétés améliorées en rhéologie dynamique. Ces dernières leur permettent de particulièrement bien résister à des sollicitations mécaniques oscillatoires, ainsi que de facilement se déformer en fluage. (Communication personnelle de Mr Meunier-laboratoires Teoxane-Genève, Suisse)
Ainsi, les gels Teosyal® RHA sont parfaitement adaptés aux injections dans les zones mobiles et dynamiques du visage, comme le démontrent les résultats à un an d’une étude clinique randomisée en hémi-visage contre des gels couramment rencontrés sur le marché. (Réf 6)
Dans cet article, et pour rester au plus proche du gel déjà testé et décrit (Teosyal® PureSense Global Action), nous avons choisi d’examiner et comparer le gel :
- Teosyal ® RHA 2, Laboratoires Teoxane-Genève, Suisse- lot n° TP30L-143601B5287 Exp : 2016-09.
Dont les indications sont identiques à celles de Teosyal® Pure Sense Global Action. On peut les résumer ainsi :
« Teosyal ®RHA 2 est indiqué pour le comblement des rides linéaires du visage, des cassures cutanées telles que les sillons nasogéniens, peu ou moyennement marqués, les rides péribuccales et rides de la glabelle. » (Réf 7)
B. Les instruments et produits
Comme pour nos études comparatives précédentes, (Réf 3, 4, 5) nous avons utilisé en juillet 2015 le matériel suivant :
- Appareil Nikon D40X, objectif AF Micro Nikkor 60mm 1 :2.8 D, pour réaliser les photographies.
Nous avons utilisé, à notre cabinet, le matériel suivant, comme pour tous nos tests antérieurs (Réf 3, 4, 5) :
- Boite de Pétri, pot pour prélèvement d’urine, mètre ruban, du sérum physiologique NaCl 0.9% -B.Braun lot n° 29554 charge 13471013 exp : 04.2016, le colorant Ecoline ® – Royal Talens- Bleu Violet n°548, une pince d’Adson, des seringues de 1 ml et des seringues Omnican®50 à aiguille 30G½ sertie, et de l’éthanol à 70°.
Nous avons utilisé au laboratoire Viollier-Genève, Suisse- du bleu de toluidine à la concentration 0.069%, ainsi que des lames et lamelles d’examen et de l’eau bidistillée, pour rincer les lames avant examen microscopique. (Réf 3, 4, 5)
Les préparations ont été examinées au microscope
- Olympus SC 100.
C. Histologie et suivi ultrasonographique (US)
Nous avons fait appel, comme pour nos études précédentes, (Réf 3, 4, 5) à l’institut de Radiologie MedImage, Genève-Suisse, et l’institut Viollier, Genève-Suisse.
Suivi ultrasonographique :
Pour les injections dans le derme réticulaire moyen sous contrôle US, nous avons utilisé le matériel suivant :
- gel RHA 2 lot n°TP30L-151705B5245 exp 2017-04
- l’appareil à US General Electric LogiQ E9® avec la tête L8 18i® (General Electric Company, Fairfield, CT 06431- USA), à la fréquence de 17 mega-Herz.
Pour une meilleure définition de l’image, un interface solide, gélifié, Aid GeitstlichPharma® lot n° 1000353 (Geistlich Pharma AG, Wolhusen- Zwitzerland) a été placé sur la surface à examiner.
Examens histologiques :
Pour les histologies : l’anesthésique choisi a été la lidocaïne 1% sans adrénaline, un punch rond de 4 mm et du fil 4/0 pour la suture.
Méthode
Comme pour les examens antérieurs d’autres gels présents sur le marché suisse, nous avons fait les tests suivants :
1. En cabinet privé
Nous avons, toujours comme précédemment, fait 2 tests très simples et reproductible, par tout un chacun, dans son cabinet.
A. Test de « cohésivité » simple
Nous avons prélevé 0.6 ml de sérum physiologique au moyen d’une seringue de 1ml, que nous avons placé dans un pot pour prélèvement d’urine. Le sérum a ensuite été coloré avec 2 gouttes du colorant Ecoline® bleu violet, prélevé grâce aux seringues Omnican®. Nous avons ensuite déposé, dans le mélange, 0.2 ml des gels à examiner, directement au travers de l’embout de la seringue originelle. Le gel a donc subi une dilution de 1/3.
Ensuite une courte agitation, par rotation manuelle du pot, a été appliquée à la préparation, pendant moins de 10 secondes. Une photographie a été réalisée. Ensuite 2 gouttes d’éthanol ont été ajoutées à la préparation, grâce toujours à une seringue Omnican®. Le mélange a subi la même agitation délicate, de quelques secondes, par rotation manuelle. Enfin le mélange final a été photographié. (Réf 3, 4, 5)
B. Test de résistance à l’élongation
0.2 ml de gel à examiner a été déposé au centre d’une boite de Pétri. À l’aide d’une pince d’Adson, nous avons essayé d’étirer gel pour tenter d’obtenir le plus long fil possible, et photographier, devant un mètre ruban, ce dernier avant qu’il ne se « casse ». (Réf 3, 4, 5)
2. Laboratoire Viollier
A. Etalement des gels
Au laboratoire, les 2 gels à tester ont été simplement étalés sur une lame, comme pour une préparation de frotti sanguin. 2 gouttes de bleu de toluidine, à la concentration 0.069%, ont été déposées sur la préparation, et laissées en contact pendant 30 secondes.
Ensuite la lame a été rincée à l’aide de 2X 1ml d’eau bidistillée, à l’aide d’une pissette, sans laver le gel étalé.
Enfin, une lamelle a été déposée sur la préparation rincée. (Réf 3, 4, 5)
B. Examen des gels au microscope
La préparation colorée ci-dessus, placée entre lame et lamelle, a été mise sous un microscope optique binoculaire pour examen et description. (Réf 3, 4,5)
3. Histologie et suivi ultrasonographique (US)
1 sujet féminin a accepté, après consentement éclairé, et dans le respect de la déclaration d’Helsinki, d’être injecté sous contrôle US, et subir une biopsie dans la région fessière.
0.2 ml de gel a été injecté sous contrôle ultrasonographique, dans le derme moyen de la région fessière, droite et gauche. La position de l’aiguille, avant l’injection, a été contrôlée et photographiée (Fig 4).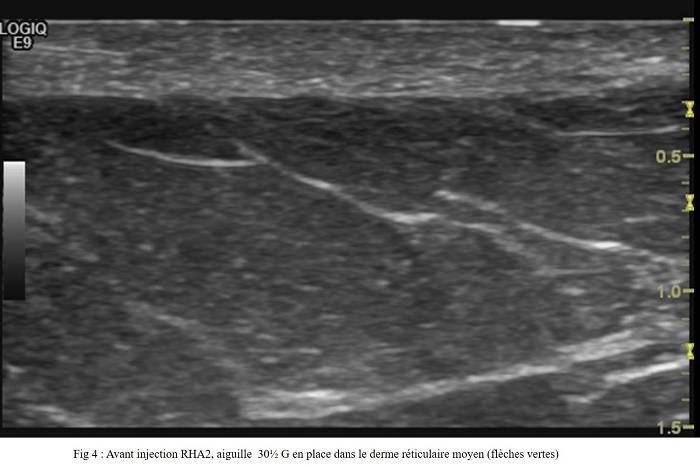
Puis le gel a été injecté, toujours sous contrôle ultrasonographique. Une photographie a été prise une fois la papule injectée, l’aiguille toujours en place dans le derme moyen, puis un autre cliché photographique a été pris une fois l’aiguille retirée. (Fig 5)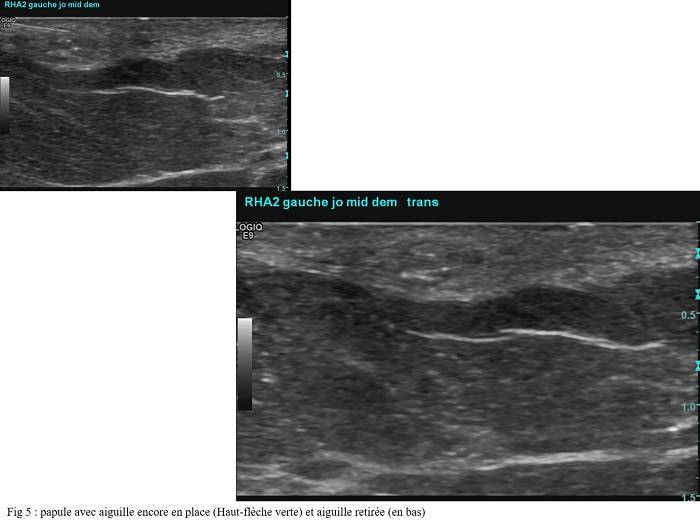
L’angle de pénétration de l’aiguille a été mesuré, ainsi que la longueur implantée de l’aiguille.
Ceci nous permet de calculer la profondeur d’injection par la formule mathématique suivante : Sinus de l’angle de pénétration multiplié par la longueur implantée de l’aiguille (en cm) = profondeur d’injection (en mm).
Ensuite, à J0, une anesthésie locale, à la lidocaïne à 1% sans adrénaline, par infiltration péri-papulaire a été pratiquée. Une biopsie au punch 4mm a été prise à droite. La zone biopsiée a été suturée au fil 4/0, et ce dernier ôté au 10ème jour.
La biopsie, immédiatement après son prélèvement, a été transportée, dans du formol, au laboratoire d’histopathologie pour préparation et examen après coloration.
A J15, le même protocole d’anesthésie et prise de biopsie a été réalisé, après contrôle échographique de la papule réalisée sur la fesse gauche.
Résultats
1. A notre consultation clinique
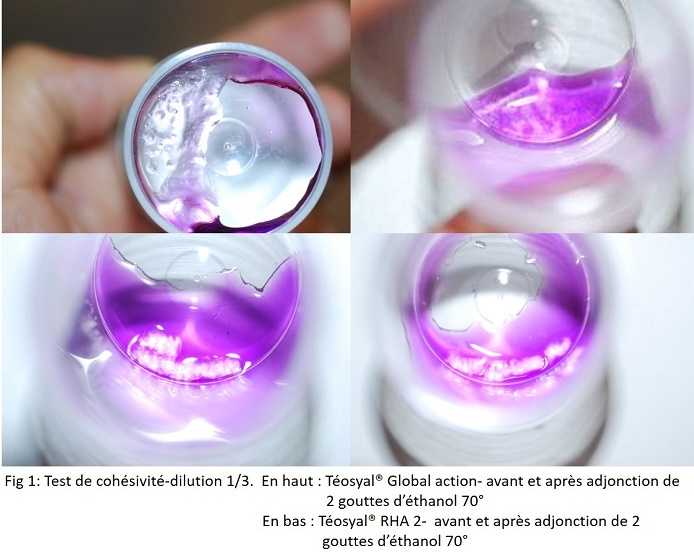
A. Test de cohésivité simple (Fig 1)
A.1. Gel Teosyal® PureSense Global Action
Après quelques secondes, le gel se délite en plusieurs amas ou « boudins » de gel. L’ajout d’éthanol 70° augmente et accélère le processus.
A.2. Gel Teosyal® RHA 2
Placé dans le sérum physiologique coloré, même après agitation manuelle de la préparation, le gel RHA 2 se présente sous la forme d’un boudin.
Après adjonction de 2 gouttes d’éthanol 70°, le gel RHA 2 reste cohésif. Tout au plus remarque-t-on un possible discret délitement.
B. Test de résistance à l’élongation (Fig 2)
B.1. Gel Teosyal® PureSense Global Action
Il nous a été impossible de réaliser une traction supérieure à 0.5 cm.
B.2. Gel Teosyal® RHA 2
Nous avons observé au cours des 4 manipulations que nous avons tenté d’effectuer avec la pince d’Adson, que :
- Soit le gel reste en un amas compact, qui s’étire jusqu’à maximum 1.5cm, puis tout en restant compact, se détache en bloc de la boite de Pétri,
- Soit se laisse discrètement étirer, mais le fil se rompt au-delà d’1 cm

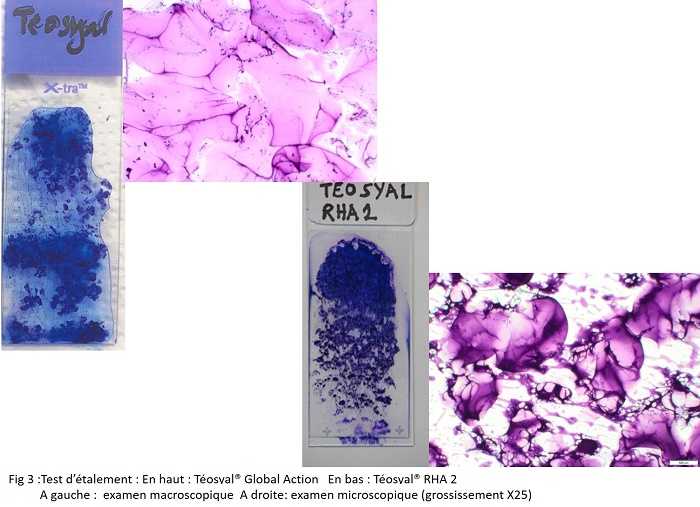
2. Laboratoire Viollier (Fig 3)
A. Teosyal® PureSense Global Action
Teosyal® PureSense Global Action présente une viscosité, une résistance à l’étalement, très importante. Après étalement sur la lame d’examen, le gel se présente comme de gros grains, très peu adhérents. Lors du rinçage à l’eau bidistillée, PureSense Global Action® est également peu adhérent.
Au microscope optique, la préparation semble très bien étalée, avec un aspect de grosses particules agglomérées. Elle ne présente pas réellement l’aspect d’un réseau complexe continu. L’image peut se rapprocher d’autres gels décrits antérieurement, mais avec des particules qui paraissent plus grosses.
Il s’agirait donc d’un gel plutôt de nature non cohésive, ou partiellement cohésif, dans ce test.
B. Teosyal® RHA 2
Dans l’ensemble, le gel Teosyal® RHA 2 a un comportement très comparable à Teosyal® PureSense Global Action. Il présente une viscosité moyenne à l’étalement sur la lame, ainsi qu’une adhérence moyenne au rinçage à l’eau bidistillée.
Au microscope, l’aspect de RHA 2 est assez proche de PureSense Global Action. Cependant, les particules mises en évidence sont de taille plus petite pour RHA® 2.
Il s’agit donc aussi d’un gel plutôt de nature partiellement cohésive, dans ce test
3. Histologie et suivi ultrasonographique (US)
A. Suivi ultrasonographique
Teosyal® PureSense Global action
A J0
Durant l’injection :
Lors de l’injection dans le derme réticulaire moyen, le gel HA PureSense Global Action, présente une importante fuite dans l’hypoderme.
Nous observons également un important épaississement du derme.
Après l’injection :
Nous observons toujours la fuite du gel dans l’hypoderme. Les papules peuvent présenter un aspect iso-ou hypo-échogène par rapport au derme avoisinant non injecté.
Son aspect interne peut être homogène ou hétérogène. Il est possible d’observer également un cône d’ombre ou un renforcement postérieur. Le gel présente une image ultrasonographique variable, non réellement caractérisée, systématisée. Il existe toujours un épaississement du derme
A J15
Il existe toujours un épaississement du derme.
L’observation ultrasonographique des papules les montre identiques à celles de J0.
Teosyal® RHA 2
Mesure échographique à J0
Les mesures observées ici sont les suivantes :
Epaisseur de l’épiderme : 0.07 mm
Epaisseur du derme avant injection : 2.70 mm
Epaisseur du derme après injection :
A gauche : 6.60 mm
A droite : 3.80 mm
Angle de pénétration de l’aiguille :
A gauche : 8°
A droite : 7°
Longueur de l’aiguille implantée :
A gauche : 7.00 mm
A droite : 10.00 mm
Calcul de la profondeur d’injection :
A gauche : 1.00 mm
A droite : 1.20 mm
Si nous additionnons les mesures échographiques de l’épiderme et du derme avant injection, nous trouvons une épaisseur totale de 2.77 mm.
Si, arbitrairement, nous considérons que les 3 couches du derme réticulaire (superficiel, moyen et profond) correspondent à 1/3 de l’épaisseur totale du derme, chaque couche a une épaisseur de 0.90 mm.
Pour être dans le derme réticulaire moyen du sujet de cette étude, il faut que l’aiguille se trouve à minimum 0.97 mm et maximum 1.87 mm.
Les calculs ci-dessus nous montrent que l’aiguille 30G incluse dans la boite de Teosyal® RHA 2 est parfaitement implantée dans le derme réticulaire moyen.
Mesures échographiques à J15
Epaisseur du derme :
A gauche : 3.0 mm
A droite : non réalisé du fait de la biopsie à J0.
Aspect ultrasonographique de l’implant
A J0
- Injecté dans le derme moyen, tant à droite qu’à gauche, le gel Teosyal® RHA2 se présente sous la forme d’une papule homogène, iso-échogène par rapport au derme avoisinant non injecté. Nous n’avons pas mis en évidence de cône d’ombre ni renforcement postérieur.
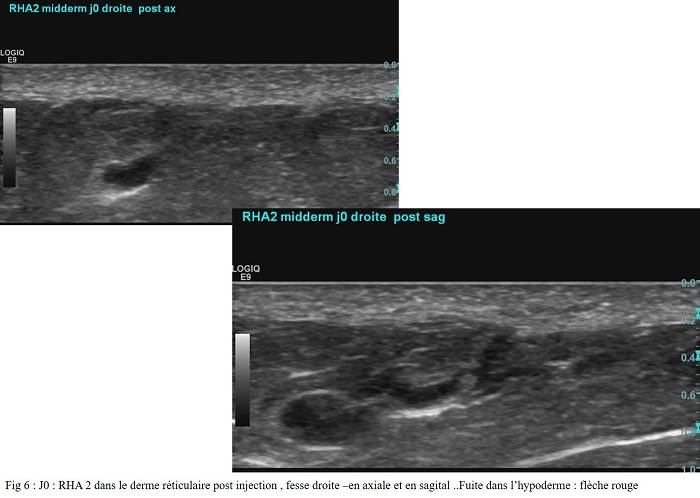
- A gauche, la papule est grande et aucune fuite dans l’hypoderme n’a été observée. (Fig 5)A droite la papule est petite. Une fuite importante dans l’hypoderme est visualisée. (Fig 6) Cette fuite explique l’épaisseur moindre du derme, mesurée sur la fesse droite, en post injection. La fuite pourrait être due à une injection à peine plus profonde
- à droite qu’à gauche (1.2 mm versus 1.0 mm). On peut aussi imaginer que la pression exercée sur le piston soit un peu plus importante… ce qui doit se produire, naturellement, lors de toute injection faite manuellement.
L’image ultrasonographique de RHA® 2 nous apparait plus systématisée que celle du gel PureSense Global Action. Le gel pourrait être qualifié de meilleure facture, ce dernier présentant ultrasonographiquement un aspect iso-échogène par rapport au derme avoisinant non injecté et la papule présentant un aspect homogène, sans zone hypo- ou hyperéchogène en son sein.
...La suite de ce contenu est réservée aux membres de l'AFME.
Pour voir l'article en entier, connectez-vous >
-
Note du comité de lecture